脂肪组织在人体内储量丰富,通过抽脂从中获得的大量脂肪干细胞(ADSCs),有自我更新增殖及多向分化潜能,可向脂肪细胞、软骨细胞、肌细胞、成骨细胞、神经细胞、神经胶质细胞及胰岛细胞分化,而且可分泌多种促血管生成因子和抗凋亡因子而抗炎、抗氧化,可抵抗氧自由基的损伤,有望成为修复受损的组织和器官的干细胞来源。
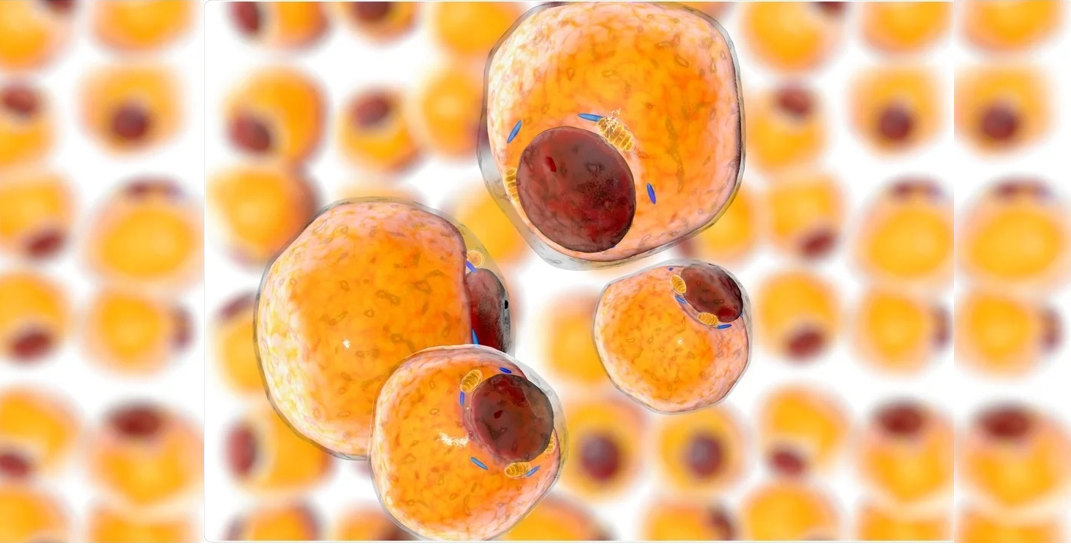
1、脂肪干细胞与间充质干细胞( MSCs)的区别
研究发现,ADSCs与MSCs在多向分化潜能、表面标记等方面,没有明显的差别,ADSCs的表面标记与MSCs非常类似,如都有CD29、CD44、CD105、CD166、CD49e;而CD31、CD34、CD45、HLA-DR、CD133、c-Kit、Lin、CD11b均为阴性;差别在于ADSCs表达CD49d,不表达CD106;而MSCs则相反。
2、脂肪干细胞分泌的细胞因子
ADSCs能分泌一定量的细胞因子,表达水平较高的细胞因子有肝细胞生长因子(HGF)、血管内皮生长因子( VEGF)、胎盘生长因子(PGF)、转化生长因子-p( TGF-(3);表达水平中等的细胞因子有成纤维细胞生长因子一2(FGF-2)、血管生成素-1(Ang-l);表达水平较低的细胞因子有血管生成素-2(Ang-2);有利于建立更好的损伤修复微环境。
3、脂肪干细胞(ADSCs)在临床上的应用
干细胞的临床应用价值主要表现在其组织修复与重建中。ADSCs能向各细胞系分化,包括中胚层源的骨细胞、脂肪细胞、软骨细胞、平滑肌细胞、血管内皮细胞、神经细胞及胰岛细胞。现在临床上主要的应用策略为转基因定向诱导、再经体外扩增干细胞后,移植入人体。
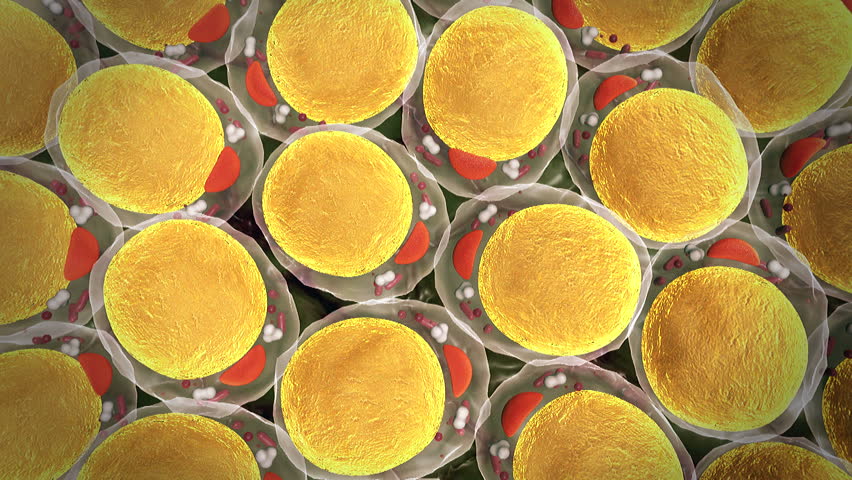
主要特点
脂肪干细胞特点:1、自体干细胞容易与自身细胞结合;2、有助于网状成纤维细胞的增殖;3、可按要求诱导组织的生长及自体干细胞的迁移。
研究发现ADSCs细胞能够在体外稳定增殖且衰亡率低,同时它具有取材容易、少量组织即可获取大量干细胞,适宜大规模培养,对机体损伤小等优点,而且其来源广泛,体内储备量大,适宜自体移植,逐渐成为近年来新的研究热点之一。
传统的脂肪移植手段由于存在免疫排斥、炎症反应等缺陷难以得到让人满意的疗效。据统计,自体脂肪组织移植到缺损部位后,通常其中40%~60%会被吸收。通过患者自身的脂肪组织内的干细胞,来构建具有完整生物学结构和功能工程脂肪组织无疑将是解决这一难题的最佳方案。如何实现从干细胞到脂肪细胞的分化,是构建工程脂肪组织不可回避的问题。早在 2001 年,Zuk 等人发现脂肪干细胞以来,就已经证明脂肪干细胞具有向脂肪、软骨、成骨、成肌等多向分化潜能。传统的成脂诱导分化采用的方法多为混合诱导剂法。成脂诱导剂的不足是带有毒性,对人体有较大危害。
除了以上通过诱导剂进行体外诱导分化外,用成熟体细胞与干细胞共培养同样可以使干细胞定性诱导分化。2000 年, Maurin 等采用间接共培养的方式,研究脂肪细胞对成骨细胞扩增和活性的影响,并证明成熟脂肪细胞对人的成骨细胞的扩增有抑制作用;但对成骨基质细胞的扩增及活性,无显着影响。2003 年Shigehisa 等采用三维胶原凝胶中共培养脂肪细胞和内皮细胞的方式研究二者间的相互作用,得出结论:内皮细胞参与到脂肪组织形成和扩增的过程当中。2007 年, Wang 等通过实验证明,鼠来源脂肪干细胞在胶原凝胶三维体系中,与OECs (Olfactory ensheathing cells-嗅鞘细胞)共培养过程中,能够分化成为OECs-like(嗅鞘样细胞)。
综上所述,通过共培养方式体外诱导干细胞定向分化已经成为研究热点。因此,本研究尝试采用trans-well 间接共培养方式,对人体吸脂来源的干细胞与脂肪细胞进行共培养,并对比传统成脂诱导剂法,考察共培养条件下干细胞成脂分化的效果。
